
Sie sind bereits Kunde oder möchten sich in einer anderen Angelegenheit an uns wenden? Treten Sie in Kontakt! Wir freuen uns auf Ihre Nachricht und melden uns umgehend zurück!
Sie haben auch die Möglichkeit, sich direkt mit einem unserer Standorte oder für internationale Anfragen mit der Holding in Verbindung zu setzen.
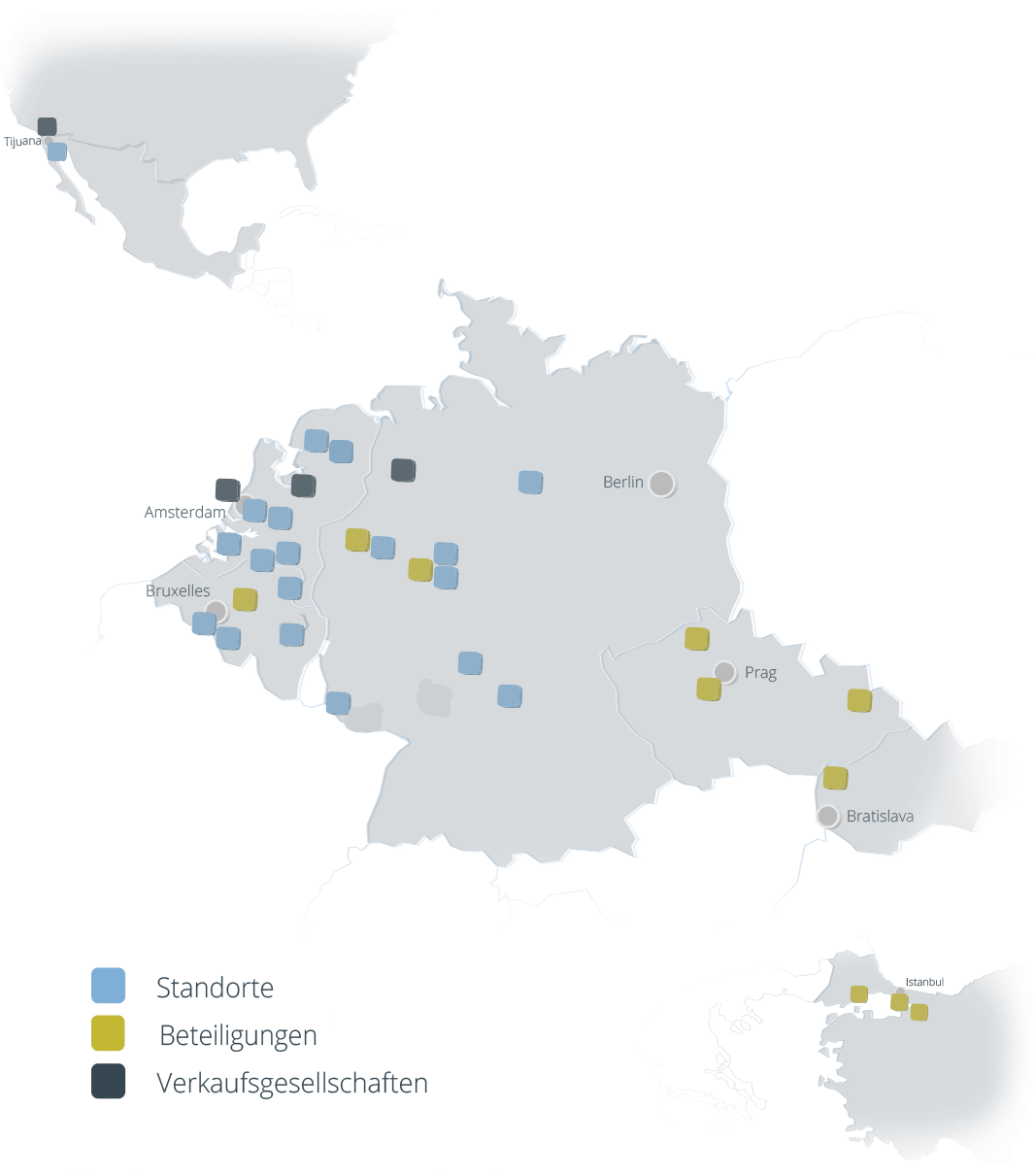
Unsere Standorte
Durch einen Klick auf den Standort kommen Sie zu den Kontaktdaten für Ihr Anliegen.
Niederlande
- Alblasserdam / NL
alblasserdam@coatinc.com - Amsterdam / NL
amsterdam@coatinc.com - Barneveld / NL
nederland@coatinc.com - De Meern / NL
demeern@coatinc.com - Groningen / NL
groningen@coatinc.com - Groningen – Pulverbeschichtung / NL
cgr.verkoop@coatinc.com - Mook / NL
mook@coatinc.com - Mook – PreGa / NL
prega.nl@coatinc.com - Roermond / NL
roermond@coatinc.com - Scherpenzeel / NL
anox@coatinc.com
Bei Anfragen zu Marketing- oder Presseangelegenheiten, wenden Sie sich bitte an den folgenden Kontakt:
Marketing & Presse
The Coatinc Company Holding GmbH
Hüttenstraße 45
57223 Kreuztal
Holding – Sie möchten Kontakt zu unserer Geschäftsführung aufnehmen?
Sitz der Geschäftsführung
The Coatinc Company Holding GmbH
Carolinenglückstraße 6-10
44793 Bochum
Telefon: +49 234 52905-0
Telefax: +49 234 52905-15
Wissensgeber 5:
In der Atmosphäre laufen zwei Vorgänge (Redoxphänomen) nebeneinander ab: die chemische und die elektrochemische Korrosion. Korrosion als Redoxphänomen ist mit den elektrochemischen Prozessen verbunden und wird daher auch „elektrochemische Phasengrenzreaktionen“ genannt. Man kann diesen Reaktionen begegnen, indem man die Abgabe von Eisen-Ionen oder von Elektronen verhindert, denn Redoxreaktionen beruhen auf einer Elektronenübertragung. Das Metall wird dabei in seine Ionen überführt. Besonders bei der gemeinsamen Verarbeitung von unterschiedlichen Metallen kommt es an den Berührungspunkten dieser Metalle daher zu schnellerer Korrosion. Es greift folgende Formel: Je höher das Redoxpotenzial, desto edler ist das Metall. Je niedriger das Redoxpotenzial, desto unedler ist das Metall. Beispielsweise nehmen die Ionen der Edelmetalle Gold, Silber, Quecksilber oder auch die von Platinmetallen bereitwilliger Elektronen auf, als die Ionen von Zink, Aluminium oder Magnesium.
Anode:
– Oxidation
– Elektronen in das Metall
– Metall lädt sich gegenüber dem Elektrolyten negativ auf.
– Potential des Elektrolyten über dem des Metalls
– Abtrag, Korrosion
Kathode:
– Reduktion
– Elektronen aus dem Metall
– Metall lädt sich gegenüber dem Elektrolyten positiv auf.
– Potential des Elektrolyten unter dem des Metalls



